唇裂和腭裂是常见的出生缺陷,在美国,大约每 1050 名新生儿中约有一个患有唇裂和腭裂。这类缺陷是由于构成嘴唇或上颚的组织未能完全连接所致,一般认为其发病是遗传和环境因素共同作用的结果。
在一项新研究中,麻省理工学院的生物学家发现面部畸形的人群中常见的一种基因变异是如何引发唇裂和腭裂的。
研究结果显示, 这种变异会减少细胞中转运 RNA(tRNA)的供应 ,而 tRNA 是蛋白质组装过程中不可或缺的分子。一旦出现这种情况,胚胎面部细胞就无法融合形成嘴唇和上颚。
“此前,从未有人建立起我们所发现的这种关联。这种名为 DDX1 的基因已知是参与 tRNA 剪接的复合体的一部分,但尚不清楚它在这个过程以及面部发育中起着关键作用。但缺乏该基因,某些 tRNA 就无法再将氨基酸转运到核糖体以合成新的蛋白质。要是细胞不能正确处理这些 tRNA,核糖体也就无法合成蛋白质了。” 该研究的主要作者、麻省理工学院的研究科学家 Michaela Bartusel 说道。
相关研究发表在 American Journal of Human Genetics 期刊。主要研究人员还包括麻省理工学院生物学副教授 Eliezer Calo。

遗传变异
唇裂和腭裂,也叫颌面裂,是全球最常见的先天性颅面畸形。病因涉及遗传和环境因素。但在大多数情况下,其潜在病因仍无法解释,从而阻碍了对疾病机制的分子理解。
通常情况下,科学家们进行全基因组关联研究(GWAS)发现影响特定疾病的遗传因素,这可以揭示出在患有某种疾病的人群中比为患该疾病的人群中更常见的变异。
对于颌面裂而言, GWAS 研究中频繁出现的一些遗传变异似乎位于不编码蛋白质的 DNA 区域 。在此次研究中,麻省理工学院的研究团队试图探究该区域的变异是如何影响面部畸形发展的。
研究表明,这些变异位于一个名为 e2p24.2 的增强子区域。增强子是与蛋白质编码基因相互作用的 DNA 片段,通过与启动基因表达的转录因子结合,进而激活这些基因。
研究人员发现,该区域与三个基因距离很近,这意味着它可能调控这些基因的表达。其中一个基因已被排除在导致面部畸形之外,另一个基因则已证实与面部畸形存在关联。在这项研究里,研究人员重点关注第三个基因 ——DDX1。
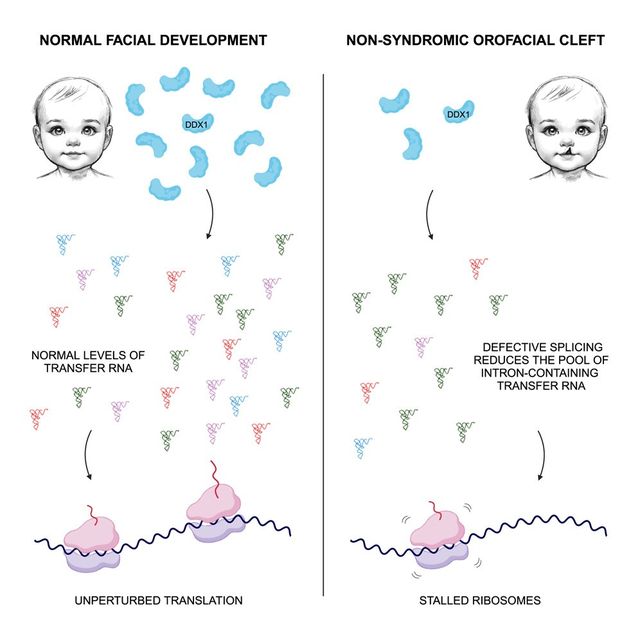
结果发现,DDX1 是 tRNA 分子所必需的,而 tRNA 分子在蛋白质合成过程中发挥着关键作用。每个 tRNA 分子都会将特定的氨基酸转运到核糖体——在那里,根据 mRNA 携带的指令,将氨基酸串联起来合成蛋白质。
人类基因组中约有 400 种不同的 tRNA,但其中只有一小部分需要进行剪接,而这些 tRNA受 DDX1 缺失的影响最大。这些 tRNA 负责转运四种不同的氨基酸,研究人员推测,这四种氨基酸在形成面部的胚胎细胞正常发育所需的蛋白质中,含量尤为丰富。
一旦核糖体需要这四种氨基酸中的某一种,却无法获取时,核糖体就会停滞,蛋白质也就无法合成。
目前,研究人员正在探索哪些蛋白质受这些氨基酸缺失的影响最大。他们还计划研究核糖体停滞时细胞内的变化情况,希望能找到一种可能被阻断并帮助细胞存活的压力信号。

功能失调的 tRNA
尽管这是首次将 tRNA 与颅面畸形建立联系的研究,但此前有研究表明,影响核糖体形成的突变也可能导致类似缺陷。还有研究显示,tRNA 合成过程受到破坏(由将氨基酸连接到 tRNA 的酶发生突变,或参与 tRNA 剪接早期步骤的蛋白质的突变引起),可能引发神经发育障碍。
“tRNA 途径中其他组成部分出现缺陷,已被证实与神经发育疾病相关。” Calo 指出,“一个有趣的相似点是,形成面部的细胞与形成神经元的细胞起源相同,因此这些特定的细胞似乎很容易受到 tRNA 缺陷的影响。”
研究人员目前希望探究与颌面出生缺陷相关的环境因素是否也会影响 tRNA 的功能。他们的一些初步研究发现,氧化应激(有害自由基的积累)会导致 tRNA 分子碎片化。胚胎细胞在接触乙醇时可能会发生氧化应激,例如胎儿酒精综合征,或者母亲患上妊娠期糖尿病。
“我认为探寻可能在基因层面导致这种情况的突变很有意义,而且未来我们还可以进一步拓展研究,看看哪些环境因素对 tRNA 功能有同样的影响,进而研究哪些预防措施能够避免 tRNA 受到影响。”Bartusel 说道。
该研究由美国国家科学基金会研究生研究计划、美国国家癌症研究所、美国国家普通医学科学研究所和皮尤慈善信托基金资助。
