地球上的每一个生命体的每一个细胞,都毫无例外地依赖碳、氢和氧三种元素构建自身的物质基础。其中,碳元素就像搭建生命大厦的基石,在有机分子的构成中担当着不可或缺的骨架角色。

正是基于这一显著特征,我们将地球上形形色色、丰富多彩的生物统一归类为碳基生命。
在生物学家和化学家们长期的研究与探索过程中,逐渐形成了一种广泛被接受的主流观点:如果在地球之外那广袤无垠的宇宙深处,某个遥远的星球上存在着生命体,那么极有可能,它们与地球生物一样,也是以碳元素为核心构建生命体系的碳基生命。
然而,科学的发展总是充满了惊喜与意外。

1891 年,德国天体物理学家朱利叶斯・席纳(Julius Scheiner)以其敏锐的科学洞察力,基于硅和碳在化学性质上呈现出的相似性,大胆地提出了一个极具创新性的观点:在构成生命的元素中,硅元素有可能替代碳元素,成为构建生命的基础元素。
一些富有想象力的科幻作者以及对宇宙充满好奇的科幻迷们,深受这一观点的启发。

他们畅想在浩瀚无垠、神秘莫测的宇宙中,各个星球的自然环境千差万别,与地球相比有着天壤之别。在如此多样化的环境下,或许存在着一些与地球生命形式截然不同的生命体,它们并非以碳为生命分子的骨架,而是以硅元素作为基础。

这种假想中的奇特生物,被赋予了一个充满科幻色彩的名称 ——“硅基生命”。
当我们回忆起中学时期在化学课堂上所学的元素周期表时,便能轻松地背诵出前面二十几个元素:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙…… 在这一长串元素的序列中,碳(C)处于第 6 位,而硅(Si)则位列第 14 位。

从地球地壳的元素含量分布来看,硅元素无疑占据着举足轻重的地位。按质量计算,它占据了地壳总质量的 27.2%,仅次于氧元素,是地壳中含量第二高的元素。
在地壳丰富多样的矿物组成中,硅酸盐矿物占据了 90% 以上的比例,硅元素在其中占据着绝对的主导地位。将我们的视野从地球拓展到更为广阔的宇宙空间,以质量为衡量标准,硅元素在众多元素中的含量排名第 8,这一数据同样显示出硅在宇宙物质构成中的可观占比。
硅元素不仅在含量方面表现突出,其化学性质与碳元素也存在着诸多相似之处。在元素周期表的第 IV 主族中,硅恰好位于碳元素的下方。这一位置关系使得它们最外层电子结构呈现出相似性,都拥有 4 个价电子。基于这一电子结构的相似性,硅与碳在一些化学行为上展现出了一致性。
例如,它们都能够与氢元素结合,形成类似有机烷的化合物。在晶体结构方面,纯硅与珍贵的钻石一样,都呈现出金刚石立方的晶体结构。这种独特的晶体结构赋予了它们坚硬的物理质地以及较高的熔点,使得它们在一定程度上具备相似的物理性质。

正是由于硅与碳在含量、电子结构以及部分化学和物理性质上存在如此多的相似特性,一些人自然而然地展开了联想与推断:既然地球上以碳元素为基础构建起了丰富多彩、繁荣昌盛的生命体系,那么在宇宙那浩瀚无边、充满无限可能的角落里,理应也存在着以硅元素为基础的生命形式,硅基生命似乎也应该在生命的舞台上拥有一席之地。
不过,尽管在地球表面硅元素的含量远远超过碳元素,但当我们将目光投向更为宏观的宇宙尺度时,却发现了一个截然不同的情况。
在银河系中,碳元素的丰度是硅元素的 7 倍之多。这一巨大差异背后蕴含着深层次的原因。碳元素的形成过程相对而言较为容易。在恒星内部那高温高压的极端环境中,通过 “三重 α 过程” 和 “CNO 聚变循环”,较轻的元素能够较为顺利地被压缩融合,从而形成更重的碳元素。
这就好比在一个高效的 “元素加工厂” 里,碳元素能够相对轻松地被 “制造” 出来。而硅元素的诞生则要艰难得多,它需要经历巨型恒星坍缩这一极为剧烈的天体物理过程。

只有在超新星爆炸那一瞬间释放出的巨大能量和极端条件下,硅元素才有机会得以产生。这种苛刻的形成条件,使得硅元素在宇宙中的含量远远低于碳元素,就如同在艰难的环境中诞生的稀有珍宝,数量自然稀少。
在地球上,纯净的碳元素能够以两种截然不同但都极具代表性的形式存在,即石墨和钻石。
石墨质地柔软,具有良好的导电性和润滑性;钻石则晶莹剔透,硬度极高,是自然界中最坚硬的物质之一。无论是石墨还是钻石,它们都展现出了极高的化学稳定性。
碳元素在常温常压下,不会轻易与氧气发生化学反应,只有在特定的条件下,例如当碳或碳化合物在氧气中燃烧时,才会发生化学反应,转化为气态氧化物 —— 二氧化碳。

从微观的原子结构层面深入剖析,碳元素的最外围有 4 个价电子,它们分别处于 2s 和 2p 轨道。这种独特的电子分布方式,使得碳元素能够与其他原子形成 4 个共价键。
并且,碳元素的共价半径仅为 77pm,较短的共价半径使得碳共价键具有较高的键能,这就如同将原子之间的连接用坚固的绳索紧紧捆绑,保证了键合的稳定性,使得碳基分子能够在各种环境下保持相对稳定的结构。
对于任何生命形式而言,其化学基础必须满足三个基本且至关重要的要求。
首先,需要具备足够的化学多样性,这就如同建造一座宏伟的建筑,需要丰富多样的建筑材料。生命活动的复杂性和多样性要求能够构建出种类繁多、功能各异的生命分子,以满足生物体内各种生理过程的需求。

其次,生命分子要兼具稳定性和一定的反应性。稳定性确保生命分子在一定时间内维持自身的结构和功能,不会轻易发生分解或变化;而反应性则是生命活动中各种化学反应得以发生的基础,只有具备反应性,生命分子才能参与到新陈代谢、物质合成与分解等关键生命过程中。
最后,合适溶剂的存在也是不可或缺的。溶剂在生命化学反应中扮演着至关重要的角色,它能够为生命化学反应提供一个适宜的环境,促进物质的溶解、运输和反应的进行,就如同化学反应的 “舞台”,为各种分子的互动和反应提供了场所。
在我们所熟悉的地球上,生命体的正常运作依赖于多种具有不同功能的化学物质协同合作。这些化学物质如同生命机器中的各个精密零件,各自发挥着独特的作用。
其中,用于制造蛋白质的氨基酸是生命活动的主要承担者 —— 蛋白质的基本组成单位。
蛋白质参与了生物体内几乎所有的生理过程,从细胞的结构支撑到生物化学反应的催化,从物质的运输到信号的传递,无处不在。用于制造核酸的糖和含氮碱基,核酸则是储存生命遗传信息的 “宝库”,掌控着生物的生长、发育、繁殖等关键生命进程,决定了生物的遗传特征和个体差异。
作为核心代谢中间体的酮酸和羟基,它们在生物体内的能量代谢和物质转化过程中发挥着不可或缺的作用,如同生命能量循环中的关键节点,推动着能量的产生、储存和利用。以及用于制造细胞膜的脂质,细胞膜如同细胞的 “城墙”,保护着细胞内部的结构和物质,维持细胞内环境的稳定,同时控制着物质的进出,确保细胞与外界环境进行有序的物质交换和信息交流。

为了组合出这些丰富多样且功能各异的化学物质,以满足生命活动的各种需求,生命体需要一套特定的元素来构建各类分子,并且在这些分子的构建过程中,需要事先搭建起一个稳固的 “脚手架”。而碳元素,凭借其独特的化学性质,成为了这个生命支架的不二之选。
碳原子拥有卓越的成键能力,它可以通过两个电子与相邻的碳原子相互连接,形成或长或短的碳链。这些碳链如同分子大厦的主梁,为构建复杂的分子结构提供了基本的框架。
同时,碳原子还能通过另外两个电子与其他不同种类的杂原子相结合,进而构建出一个庞大而复杂的大分子。在这个大分子体系中,碳链构成了稳定的支架结构,为整个分子提供了基本的框架和稳定性,就如同建筑中的钢筋结构,支撑起了整个建筑的重量和形状。而与之结合的杂原子则如同大厦中的各种功能性部件,赋予了每个分子独特的化学活性和功能特性。
这种由碳支架和杂原子共同构建的分子体系,不仅使得生命体能够制造出大量具有不同功能的分子,满足生命活动在物质运输、信号传递、催化反应等方面的多样化需求,而且碳支架相对稳定的特性,保证了分子在一定环境条件下的结构完整性,同时杂原子所提供的化学功能又为每个分子赋予了独特性,使得生命分子能够精准地执行各自的生物学功能。
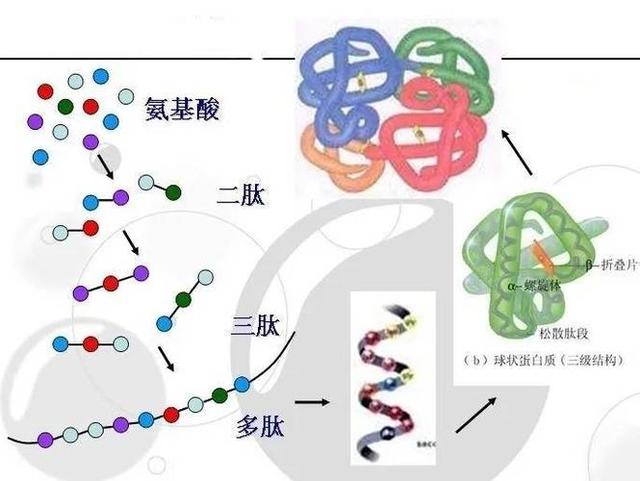
例如,在蛋白质分子中,碳链构成了多肽链的主链结构,而连接在碳链上的不同氨基酸残基则通过其独特的化学基团,赋予了蛋白质不同的三维结构和功能,如酶的催化活性、抗体的免疫识别功能等。在核酸分子中,碳骨架支撑着含氮碱基和磷酸基团,形成了双螺旋结构,而碱基之间的互补配对则决定了遗传信息的储存和传递方式。
尽管硅元素在很多方面与碳元素有着相似之处,并且在地球上的含量也相当丰富,但令人困惑的是,在地球上,我们从未发现哪怕一种以硅为基础的生命形态,甚至连一块纯净的硅单质在自然环境中都极为罕见。
这一奇特现象背后的原因,需要从硅原子本身的结构和性质进行深入探究。
硅的原子半径相较于碳要大,其共价半径达到了 117pm,明显长于碳的 77pm。硅原子的四个外围电子,两个位于 3s 轨道,两个在 3p 轨道。这种电子轨道分布以及较大的原子半径,导致硅原子的化学性质与碳有着显著的差异。

较长的键长和不同的键角使得硅原子比碳原子更加活泼,其形成的共价键稳定性也远不如碳。硅原子的这种活泼性,使得它在自然环境中很容易与氧气发生化学反应。一旦与氧气接触,硅原子会迅速被氧化,形成固态的二氧化硅。
而二氧化硅,正是我们日常生活中常见的砂子的主要成分。这就是为什么在地球上,我们几乎无法找到纯净的硅单质,所见到的大多是二氧化硅以及各种硅酸盐矿物,硅元素仿佛被 “禁锢” 在了这些化合物之中,难以以单质的形式存在。
与碳、氮、氧和氢等常见元素相比,硅具有更强的正电性。
这种正电性会在硅原子周围形成一个电子 “洼地”,使得硅原子在与其他非金属元素形成化学键时,键的极化现象更为显著。极化后的化学键使得以硅为核心的分子更容易受到亲电和亲核攻击,分子结构变得不稳定。
尤其是在与水接触时,硅化合物相较于碳化合物更容易发生水解反应。水解反应会破坏硅化合物的分子结构,使其分解为更简单的物质,无法维持稳定的分子形态。

在宇宙中,氢和氧是最为丰富的两种元素,并且天文学家通过长期的观测和研究已经证实,水分子在宇宙中广泛存在。无论是在星际空间的尘埃云中,还是在行星的大气层和表面,都能发现水分子的踪迹。在这样一个富含氢、氧以及水的宇宙环境里,硅元素面临着严峻的挑战。
一方面,它很容易被氧化变成固体,失去参与复杂化学反应的活性,就如同被 “封印” 在了固态的氧化物中。
另一方面,即便形成了硅基分子链,也会迅速被水分子破坏,难以维持稳定的分子结构。这就使得硅元素在化学多样性方面受到极大限制,根本无法像碳元素那样,通过构建多样化的分子结构,为生命的诞生和发展提供物质基础。
因此,在有水存在的环境中,硅无法担当起构成大分子骨架的重任,而仅仅只能作为碳分子链条中的杂原子存在,其地位和作用与碳元素在生命体系中的核心地位不可同日而语。例如,在一些复杂的有机硅化合物中,硅原子虽然能够参与分子的构成,但由于其化学性质的不稳定,这些化合物的稳定性和反应性都受到了很大影响,无法像碳基化合物那样,在生命过程中发挥广泛而重要的作用。

许多人仅仅从表面上看到硅与碳在元素周期表中的位置相近,以及一些基本化学性质的相似性,就轻易地认为硅有可能像碳一样成为生命的基础元素。
然而,通过对它们元素性质的深入分析,我们清晰地认识到,硅与碳只是一对 “假双胞胎”,它们之间的相似之处仅仅停留在较为肤浅的层面,而差异却是全方位且显著的。
在化学稳定性方面,碳与硅所需要的外部条件几乎截然相反。碳能够在相对温和的环境中形成稳定的化学键,构建出丰富多样且稳定的有机大分子,为生命的起源和发展提供了坚实的物质基础。而硅要想稳定地形成复杂有机大分子,所需要的自然条件在目前已知的宇宙环境中并不存在。
硅基分子在面对氧气和水等常见物质时,极易发生化学反应,导致分子结构的破坏和功能的丧失,无法满足生命化学基础所要求的稳定性和化学多样性。
从宇宙元素丰度的角度来看,碳在宇宙中的含量比硅丰富得多。这意味着在宇宙物质的原始构成中,碳元素具有更大的优势,更容易参与到生命分子的构建过程中。

同时,氢、氧以及水在宇宙中广泛分布,而科学家们通过对宇宙光谱的长期观测和分析,至今都没有接收到任何能够支持硅基生命存在的化学信息。相反,大量的研究证据表明,高分子碳基化学物质在宇宙中的分布极为广泛。
从星际空间的尘埃云到行星的表面,都能检测到各种碳基化合物的存在。这进一步从侧面印证了,在宇宙中,碳基生命存在的可能性远远高于硅基生命。例如,在一些彗星和陨石中,科学家发现了多种复杂的碳基有机化合物,这些化合物可能是生命起源的重要前体物质。而对于硅基生命,目前尚无任何确凿的证据表明其存在的可能性。
即便我们大胆假设在遥远的地外星球上存在着适宜生命繁衍的条件,从元素的化学性质和宇宙环境的实际情况来推断,这些星球上诞生的生命首先也更有可能是碳基生命。
在这样的星球环境中,硅元素要么会被氧化成石头,深埋于地底,无法参与生命分子的构建。要么会在有水的环境中发生水解反应,失去参与构建生命分子的机会,其原子结构和化学性质决定了它在常见的宇宙环境中难以形成稳定且多样化的生命分子。

又或者仅仅存在于科幻小说家充满想象力的文字之中,成为人们对未知生命形式的一种美好遐想。因此,基于目前对宇宙元素性质和分布的了解,碳基生命在宇宙生命形式中占据主导地位,而硅基生命的存在仍然只是一种充满科幻色彩的假设,有待未来科学的进一步探索和验证。
